Kemialliset ominaisuudet
Yleisimmin käytettyjä kromiyhdisteitä ovat erilaiset kromaatit ja dikromaatit. Kun punainen kromi(VI)oksidi CrO3 liukenee veteen, muodostuu hapan punaoranssi dikromaattiliuos.
Kun dikromaattiliuos tehdään emäksiseksi, väri muuttuu keltaiseksi liuokseen muodostuvien kromaatti-ionien takia.
Kromi muodostaa yhdisteitä kolmella eri hapetusluvulla: +II, +III ja +VI. Cr2+-ioni on voimakas pelkistin vesiliuoksissa.
Kromi(VI)ioni on hyvä hapettaja, erityisesti happamassa liuoksessa.
Sen hapetuskyky kasvaa liuoksen pH:n laskiessa.
Kromiiteissa ja kromin suoloissa kromi esiintyy hapetusluvulla +III. Useimmat näistä yhdisteistä ovat vihreitä mutta osa on punaisia ja sinisiä.
Kromaateissa ja dikromaateissa kromin hapetusluku on +VI. Kaliumdikromaatti on punainen vesiliukoinen kiinteä aine, joka liivatteeseen sekoitettuna tekee valoherkän pinnan, jota käytetään hyödyksi valokuvauksessa. Kromaatit ovat yleensä keltaisia. Niistä tunnetuin on lyijykromaatti, jota käytetään keltaisen pigmenttinä eli kromin keltaisena. Kromin vihreä pigmentti on sekoitus kromin keltaista ja Preussin sinistä.
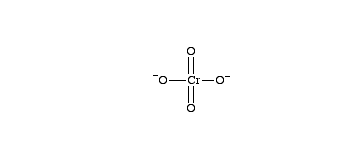
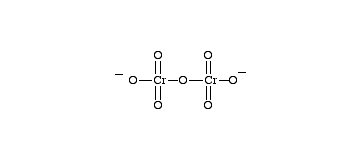
Kromaatti- ja dikromaatti-ionit. Lähde: www.chemthes.com.