Vesimolekyyli
Meriveden kemiallinen koostumus
Merike Kesler
Iina Oliver
Helsingin yliopisto
2003
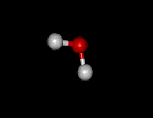 |
Tetraedrissä orbitaalien välinen kulma on 109,4o, mutta vedessä se on 104,5o. Tämä johtuu happiatomin lähellä sijaitsevan sitoutumattoman elektroniparin voimakkaasta poistovoimasta. Voimakkaan poistovoiman ja kovalenttisen (O-H) sidoksen yhteisten elektroniparien välisen vuorovaikutuksen seurauksena happiatomiin liittyneet vetyatomit työntyvät hieman lähemmäksi toisiaan muodostaen vesimolekyyliin (H-O-H) kulman 104,5o. |
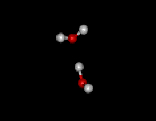 |
Elektronien esiintymistodennäköisyys on hieman suurempi happiatomin ympäristössä ja siitä johtuu vesimolekyylin poolisuus. Tämä aiheuttaa vuorovaikutuksen - vetysidoksen - veden happiatomin ja kahden sen lähistöllä olevan vesimolekyylin vedyn välillä.
|
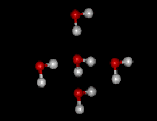 |
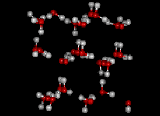
Vesimolekyylit voivat liittyä vetysidosten kautta toisiinsa suureksi löyhäksi molekyyliparveksi. Vetysidosten vahvuus on noin kymmenesosa tavallisen kovalenttisen O-H-sidoksen vahvuudesta. Vetysidoksen purkamiseen tarvittava energia on n.
10 kJ/mooli. Vesi on erinomainen väliaine hidastamaan lämpötilamuutoksia luonnossa. |
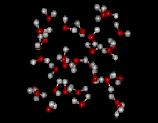 |
Vetysidosten ansiosta vesi on myös erinomainen liuotin. |
 |
Syksyllä veden jäätyessä vapautuu runsaasti lämpöenergiaa, joka hidastaa jäähtymisprosessia. Keväällä sulamisessa sitoutuu vastaavasti energia, mikä puolestaan hidastaa lämpenemistä. Makean veden tiheysmaksimin lämpötila +4oC aiheuttaa kerrostumisen järvivesissä niiden lämmetessä. Jään muodostumisen nopeudella ja ajankohdalla on suuri ekologinen merkitys. Veden suolapitoisuus vaikuttaa voimakkaasti veden tiheyteen ja samalla se alentaa veden jäätymispistettä. |