Kiehtovaa kemiaa tietokoneella
Navigointi
|
Jalokaasujen kemiaa?Jalokaasujen jalosukuisuuden taivaalle ilmestyi mustia pilviä 1933, jolloin Linus Pauling tutkiessaan kemiallisten sidosten muodostumista ymmärsi, että tarpeeksi elektronegatiivinen (elektroneja puoleensa vetävä) atomi voisi ryöstää elektronin jalokaasuatomilta. Linus Pauling ennustikin, että on mahdollista muodostaa kemiallinen sidos ksenonin ja fluorin välille, kenties myös kryptonin ja fluorin välille - fluorihan on kaikista elektronegatiivisin atomi jaksollisessa järjestelmässä. Kokeellisesti Paulingin ideoita oli kuitenkin hankala varmentaa ja vasta muutama vuosikymmen myöhemmin (1962) Neil Bartlett huomasi aukon jalokaasujen reagoimattomuuden muurissa. Hän onnistui muodostamaan yhdisteen ksenonista ja platinaheksafluoridista ja samalla tuli antaneeksi alkusysäyksen jalokaasujen synteesikemialle: sopivasti kutiteltuna jalokaasut voidaan saada reagoimaan useiden eri atomien kuten hapen, fluorin ja kloorin kanssa.
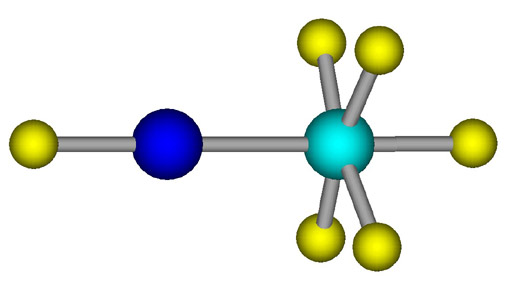
FXePtF5-molekyyli Nykyään tunnetaan monia jalokaasujen muodostamia molekyylejä, joista monet muodostavat värikkäitä ksenonia ja fluoria sisältäviä ionisia kiteitä. Ksenonin ja kahden fluoriatomin muodostama yhdiste ksenondifluoridi (XeF2) on jopa kaupallisesti saatavilla ja teollisuuden käytössä mm. etsaustöissä. Fluoripitoisia jalokaasuyhdisteitä käytetään myös laajasti orgaanisessa kemiassa, kun halutaan tehdä uusia fluorattuja yhdisteitä. Ensimmäiset täysin ilman fluoria olevat jalokaasumolekyylit valmistettiin 1995 Helsingin yliopiston kemian laitoksella. Nämä ns. jalokaasuhydridit sisältävät aina vetyatomin sitoutuneena jalokaasuatomiin. Molekyyliperheen yleinen rakennekaava on HRgX, jossa H on vetyatomi, Rg on jalokaasuatomi ja X on jokin elektronegatiivinen atomi tai atomiryhmä. Vuoden 2003 kesään mennessä tämän molekyyliperheen jäsenten lukumäärä on 17, joista ksenonyhdisteitä on 13. Tunnetut ksenonhydridit:
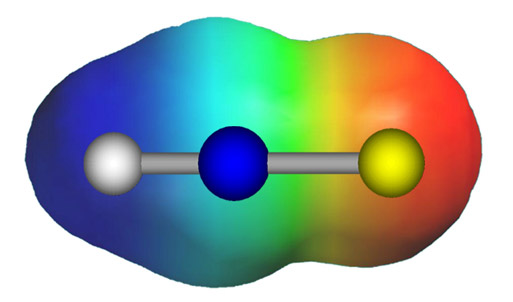
Tunnetut kryptonhydridit: Bartlettin ensimmäisestä jalokaasumolekyylistä lähtien jalokaasujen kemia on ollut pääosin kryptonin, radonin ja erityisesti ksenonin kemiaa. Viimeisimpänä rajapyykkinä jalokaasujen kemiassa on ollut argonin saaminen mukaan kemiallisten yhdisteiden muodostajien joukkoon. Ja maailman ensimmäisen argonyhdisteen, hydridoargonfluoridin (HArF) suunnitteluun käytettiin molekyylimallinnusta. Molekyylin ensimmäinen ennuste ilmestyi 1995 ja molekyyli valmistettiin kokeellisesti vuosituhannen vaihteessa - ja sen kokeellisesti havaitut kemialliset ominaisuudet olivat hyvin lähellä laskennallisesti ennustettuja ominaisuuksia.
|