Kiehtovaa kemiaa tietokoneella
Navigointi
|
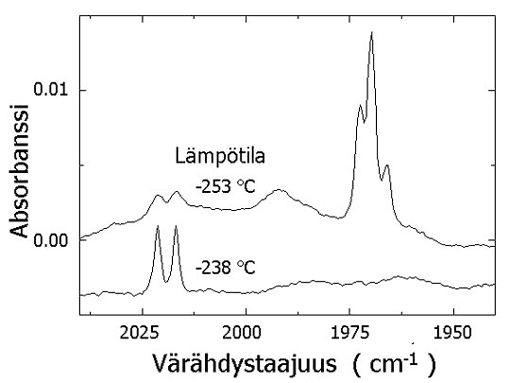
HArF:n elämää jalokaasukiteessäHArF on valmistettu alhaisen lämpötilan matriisissa eikä sitä vielä toistaiseksi ole pystytty tekemään kaasutilassa ilman kiinteää argonkidettä molekyylin ympärillä. Argonkide ei kuitenkaan ole syypää molekyylin muodostumiselle, sillä molekyyli muodostuu itsestään, ilman mitään estettä, vety- ja fluoriatomien kohdatessa. Molekyyli tuntee ympärillä olevien muiden argon-atomien vaikutuksen, sillä kiinteässä kiteessä se on monien argon-atomien puristuksessa. Ympäristön vaikutukset voidaan havaita kokeellisesti HArF:n värähdysspektrin pieninä muutoksina kuten alla olevasta kuvasta voidaan havaita.
Kuvassa (yllä) on esitetty HArF-molekyylin värähdysspektri lämmitettäessä kylmää näytettä ensin 20 astetta, jolloin tulee näkyviin vahva HArF:n H-Ar venytysvärähdys. Nostettaessa lämpötilaa vielä 15 astetta lisää, ensin muodostunut värähdys häviää ja sen tilalla tulee näkyviin uusi värähdys noin 2020 aaltoluvun (cm-1) kohdalla. Tämä ilmiö johtuu HArF-molekyylin ympärillä olevien argon-atomien lämpöliikkeestä, jolloin korkeammassa lämpötilassa kide mukautuu HArF-molekyylin läsnäoloon paremmin. Kokeellisesti ei saada tietoa minkälaisista paikallisista HArF/Ar-rakenteista kyseiset signaalit tulevat, mutta molekyylimallinnuksen avulla voimme tarkastella tarpeeksi suurta kidettä, jotta saamme mikrotason tietoa ilmiön synnystä.
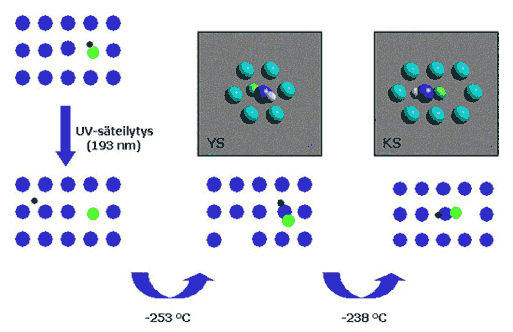
Voimakenttälaskujen avulla voimme mallintaa HArF-molekyyliä argon-kiteessä. Yllä olevat kuvat on saatu tutkimalla HArF-molekyylin lähinaapureita kiteessä, jossa on yhteensä noin 1400 atomia. Molekyylimallinnus ehdottaa, että HArF voi ottaa kolme erityyppistä paikkaa argon-atomien keskellä. Näistä yksi on paikka, jossa HArF on sijoittunut yhden ainoan argon-atomin tilalle, ns. yksisubstitutionaalinen (YS) paikka. Mikäli molekyylin sallitaan korvata kaksi argon-atomia, voi se olla sijoittuneena lineaarisesti aukossa (kaksisubstitutionaalinen, KS) tai kääntyneenä vinoittain, jolloin molekyylin viereen jää aukko (T-muotoinen kaksisubstitutionaalinen paikka, T-KS). Energeettisesti keskimmäisen kuvan esittämä KS-rakenne on kaikkein suotuisin olotila HArF-molekyylille kiinteässä argonissa.
Kuvassa on esitetty HArF-molekyylin syntymekanismi. Vasemmalla ylhäällä HF-molekyyli eristetään kiinteään argoniin. Ultraviolettisäteilytyksen vaikutuksesta HF-molekyyli hajoaa ja tuottaa vety(H) ja fluori(F) -atomeja. Lämmitettäessä näytettä H ja F -atomit lähtevät liikkeelle ja törmäävät muodostaen HArF-molekyylin. Lämmitystä jatkettaessa HArF-molekyylin ympärillä olevat muut argon-atomit sopeutuvat HArF-molekyylin läsnäoloon lämpöliikkeen ansiosta. HArF-molekyylin tutkimuksissa molekyylimallinnusta on siis käytetty ensiksi ennustamaan molekyylin olemassaolo ja sen molekulaariset ominaisuudet. Molekyyliä tehtäessä laskennallisia menetelmiä on käytetty varmistamaan kokeellisesti havaittuja ominaisuuksia, erityisesti vertailemalla molekyylin kokeellisesti havaittuja ja teoreettisesti laskettuja värähdysliikkeitä. Lisäksi molekyyliin vaikuttavia havaittuja ympäristömuutoksia on voitu mallintaa ja selittää laajamittaisten molekyylisimulaatioiden avulla. HArF on hyvä esimerkki monipuolisesta molekyylimallinnuksesta, joka sekä tukee kokeellista tutkimusta että ehdottaa uusia mahdollisuuksia. Ilman molekyylimallinnusta HArF-molekyyli saattaisi olla edelleen historian hämärässä odottamassa löytämistään.
|